
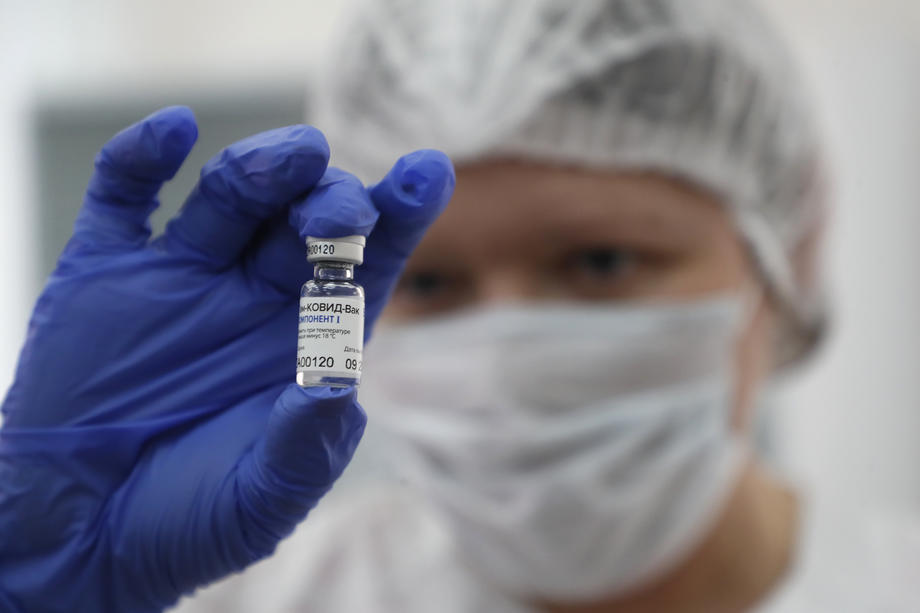
Hann sagði að RDIF hafi nú þegar samið við ítölsk, spænsk, frönsk og þýsk fyrirtæki um að hefja framleiðslu á bóluefninu en RDIF ber ábyrgð á alþjóðlegri markaðssetningu bóluefnisins.
Evrópska lyfjastofnunin, EMA, hefur nú þegar mælt með að fjögur bóluefni verði samþykkt til notkunar innan ESB og hefur framkvæmdastjórn ESB samþykkt þessi fjögur bóluefni. Þetta eru bóluefnin frá Pfizer/BioNTech, Moderna, AstraZeneca og Johnson & Johnson.
Ekki hefur verið sótt um markaðsleyfi fyrir Sputnik V hjá ESB en EMA byrjaði í síðustu viku rannsókn á tilraunagögnum bóluefnisins. Það getur síðar meir stuðlað að því að það fái markaðsleyfi í ESB.
Dmitrijev sagði að samningarnir opnuðu á möguleikann á að Sputnik V bóluefni geti komið á markað í Evrópu þegar „EMA samþykkir það“. Það er þó ekki EMA sem samþykkir að nota megi bóluefni í ESB en stofnunin kemur með ráðleggingar til framkvæmdastjórnarinnar sem hefur lokaorðið. Það ferli tekur yfirleitt skamman tíma og oft hefur framkvæmdastjórnin samþykkt það sem EMA leggur til samdægurs.
Ítalski miðillinn Sole 24 Ore hafði eftir embættismanni hjá EMA að stofnunin verði væntanlega ekki tilbúin með ákvörðun í máli Sputnik V fyrr en í maí.
Vísindaritið The Lancet birti í febrúar niðurstöður sem sýna að Sputnik V bóluefnið sé öruggt og hafi rúmlega 90% virkni.
Búið er að bólusetja 3,5 milljónir með bóluefninu í Rússlandi. Slóvakía og Ungverjaland, bæði ESB-ríki, hafa keypt bóluefnið og Tékkar hafa sýnt því áhuga.